-
由于全球气候变化严峻,实现低碳发展对技术升级提出了新的目标和要求。有研究表明,在污水生物处理过程中产生二氧化碳(CO2)、氧化亚氮(N2O)和甲烷(CH4)等温室气体[1]。污水生物脱氮过程是N2O的直接排放源,N2O大气升温效应是CO2的298倍[2],其同时与臭氧层的破坏、全球变暖、酸雨等密切相关[1]。在污水处理过程中N2O的排放量可占到污水厂碳排放量的83%[3],因此,N2O减排是降低污水厂碳排放的重要环节[4]。N2O主要产生于硝化、反硝化反应过程,不同生物处理工艺N2O排放量不同,大型污水厂中N2O排放变化幅度大,排放因子为0~14.6%[5]。韩海成认为A2O工艺中好氧曝气池是主要N2O排放源,排放因子为6.34%~8.83%[6]。同时N2O排放受进水水质、曝气量、溶解氧浓度、进水策略等因素影响[3]。较高的进水负荷会增加硝化反应N2O排放,当污水碳氮比较低时,反硝化反应碳源不足,N2O排放量升高[3]。一氧化氮(NO)作为反硝化反应N2O转化的前体物,有助于N2O排放规律的解析[6]。
在高品质出水与碳减排双向约束下,需要寻求更为高效、低碳的污水处理技术。厌氧氨氧化工艺(anaerobic ammonia oxidation, anammox)由于其运行能耗低、无需外加碳源等优点,在生物脱氮方面已成为研究热点[7-9]。厌氧氨氧化反应中由肼(N2H4)脱氢产生N2,因此,理论上厌氧氨氧化反应不产生N2O。膜曝气生物膜反应器(membrane aerated biofilm reactor, MABR)属于膜载体生物膜反应器(membrane-supported biofilm reactor, MSBR)的一种。DUAN等[3]指出MABR是一种低N2O排放技术,空气或氧气通过透气膜渗透,有机物和氨氮在混合液侧向生物膜内部扩散,形成“逆向传质”的生物膜结构[10],该结构利于控制亚硝化反应[11]。MABR具备实现亚硝化-厌氧氨氧化反应的有利条件。通过本课题组前期研究表明,MABR耦合厌氧氨氧化工艺可实现低碳氮比生活污水中的高效脱氮[12]。MABR和厌氧氨氧化技术具备较低温室气体排放潜力,然而其温室气体排放特性尚缺乏相关参数报道。
针对生活污水处理过程中碳减排需求,本研究构建了一体式MABR,采用厌氧氨氧化工艺处理低碳氮比生活污水,在实现高效脱氮的基础上分析了N2O、NO、CH4等气体的排放规律,以期为污水处理碳减排提供参考。
-
本实验装置示意图如图1所示。反应器整体材质为有机玻璃,有效容积为3 L。反应器内放置由PVDF中空纤维膜丝构成的膜组件,膜丝直径为1.8 mm,长为380 mm,膜孔径为0.1~1 µm,膜表面积为0.19 m2。气泵连接膜组件并向膜丝曝气,进气管连接转子流量计和压力计,气体流量为120~150 L·min−1,控制曝气阶段DO质量浓度约0.2 mg·L−1。出水通过蠕动泵流入出水箱。该反应器整体采用时控开关控制,以实现反应器的自动运行。
-
该反应器的运行周期为12 h,包括10 min进水,120 min厌氧阶段,480 min好氧阶段(间歇曝气50~70 min 开/50~70 min 关),40 min沉淀阶段,10 min出水和60 min静置,排水比为43.3%,HRT为20.8 h。曝气时控制反应器内DO≤0.2 mg·L−1,维持反应器内混合液温度为27~30 ºC。实验前接种厌氧氨氧化污泥,并实现了挂膜和稳定运行,实验前经15N同位素示踪分析,厌氧氨氧化脱氮贡献均值为70%[12]。
本实验共运行了60 d,分为2个阶段:第1阶段为模拟生活污水(30 d),第2阶段为实际生活污水(30 d),2个阶段之间没有间隔,未对膜进行任何处理,运行控制参数相同。第一阶段的模拟生活污水由NH4Cl、CH3COONa、NaHCO3和KH2PO4以及微生物生长所需的微量元素[13]配置而成。第2阶段的实际生活污水,取自北京市某城市污水处理厂格栅、沉砂后(进入生化处理池前)的污水。不同阶段的进水水质见表1。
-
1)气态气体的采样与测试。2个阶段分别选取第23天和第49天对稳定运行的MABR装置进行气体和水质样品采集。利用动态箱气体监测法[14](图1),将反应器上部顶空空间密闭,通过气泵和空气流量计向反应器顶空连续通入空气,空气流量约5.5~8.3 L·h−1(空气流量为顶空空间每小时气体循环10~15次)。同时通过出气管连接气袋采气,收集的气体以及室内空气本底样品采用气相色谱(7890A,安捷伦)分别测试CH4、N2O浓度,CH4检出限为0.3 mg·m−3,N2O检出限为0.05 mg·m−3。并采用Thermo 17i 氨分析仪对气体中一氧化氮(NO)浓度进行测试,NO检出限为0.01 mg·m−3。
2)溶解态N2O的采样与测试。采用60 mL医用注射器,从反应器中取样30 mL水样,再抽取30 mL高纯氦气,在注射器中使水样上方形成气室,并用三通封闭注射器顶部。在室温下将注射器剧烈振荡5 min,使溶解性气体析出进入注射器上部,静置10 min,使气液两相达到平衡,最后将注射器上部的气体推入12 mL真空瓶,利用气相色谱测定其浓度[15]。溶解性气体样品约120 min采集1次。
3)水质指标的检测。水样经过0.45 µm的滤头过滤后,NH4+-N、NO2−-N和NO3−-N采用在紫外分光仪(TU-1901,China)中进行测定,化学需氧量(COD)采用快速消解法进行测定。三维荧光采用荧光分光光度计(Hitachi, F-7000, Japan)测定。
4)气体的排放通量与排放因子的计算。污染物(COD、NH4+和TN)去除率采用式(1)计算;气体的排放通量采用式(2)[16]计算;排放因子(emission factor, EF)采用式(3)计算。
式中:η为污染物去除率,%;Cinf和Ceff分别为进水和出水质量浓度,mg·L−1。
式中:F为气体排放通量,mg·(m2·h)−1;A为覆盖液体面积,m2;Q为气体外溢流量,m3·h−1;C2为集气罩出气口的气体质量浓度,mg·m−3;C1为环境气体质量浓度,mg·m−3。
式中:Qemission为温室气体释放量,mg·h−1;ωemission为温室气体排放因子(即排放量占进水COD或NH4+-N的比例),%;Cin为进水中COD或NH4+-N质量浓度,mg·L−1;Qin为进水流量,L·h−1。
-
两阶段进水水质和去除如表1所示。阶段1(模拟生活污水阶段)进水COD值为115 mg·L−1左右,出水COD值为17 mg·L−1,COD去除率达到85.24%。阶段2(实际生活污水阶段)进水COD值约为64 mg·L−1,出水COD值降低至16 mg·L−1左右,COD去除率达到75.39%左右。2个阶段COD均达到很好的去除效果,但阶段1的COD的去除率更高。这可能与该阶段进水COD值较高有关,阶段2进水COD组分复杂,生物处理COD去除可能偏低。在不同进水条件下,MABR出水COD值相似,表明该反应器可耐受不同进水COD变化。
为了阐述有机物在反应器内变化对水样中溶解性组分,进行了三维荧光分析,结果如图2所示。阶段1的进水主要以溶解性微生物代谢产物为主,且荧光组分单一,经过反应器处理后该组分有下降趋势。阶段2的进水水质较于阶段1更为复杂,主要荧光成分包括溶解性微生物产物(250 nm<Ex<280 nm,280 nm<Em<380 nm)、芳香蛋白类物质Ⅰ(220 nm<Ex<250 nm,280 nm<Em<330 nm)以及芳香蛋白类物质Ⅱ(220 nm<Ex<250 nm,330 nm<Em<380 nm )[17]。其出水中溶解性微生物代谢产物、芳香蛋白类物质Ⅰ以及芳香蛋白类物质Ⅱ均有明显的去除效果。杨金强[18]的研究表明,在城市生活污水处理过程中,芳香蛋白类物质的去除可能与微生物降解作用有关,而溶解性微生物产物的减少可能由于好氧曝气阶段的微生物氧化作用。
不同进水条件下反应器进、出水氮素浓度变化和去除率如表1所示。阶段1(0~30 d)中,进水NH4+-N质量浓度为(39.1±0.92) mg·L−1,C/N为3.00±0.14。出水NH4+-N、NO2−-N和NO3—N质量浓度分别(3.89±2.22)、(0.07±0.01)、(9.92±5.68) mg·L−1,NH4+-N和TN去除率分别为90.10%和64.3%。阶段2(30~60 d)中,进水NH4+-N质量浓度为(38.44±4.27) mg·L−1,C/N为1.67±0.07。出水NH4+-N、NO2−-N和NO3−-N质量浓度分别为(1.39±1.15)、(0.03±0.02)和(5.4±3.77) mg·L−1,NH4+-N和TN去除率分别为96.39%和81.88%。2个阶段均实现了较好的NH4+-N和TN去除,在较低的C/N条件下,TN实现了高效去除。厌氧氨氧化利用NH4+-N和NO2−-N发生自养脱氮,有利于低碳氮比污水脱氮[19]。在MABR中通过亚硝化-厌氧氨氧化反应以及反硝化反应实现总氮去除[14]。
-
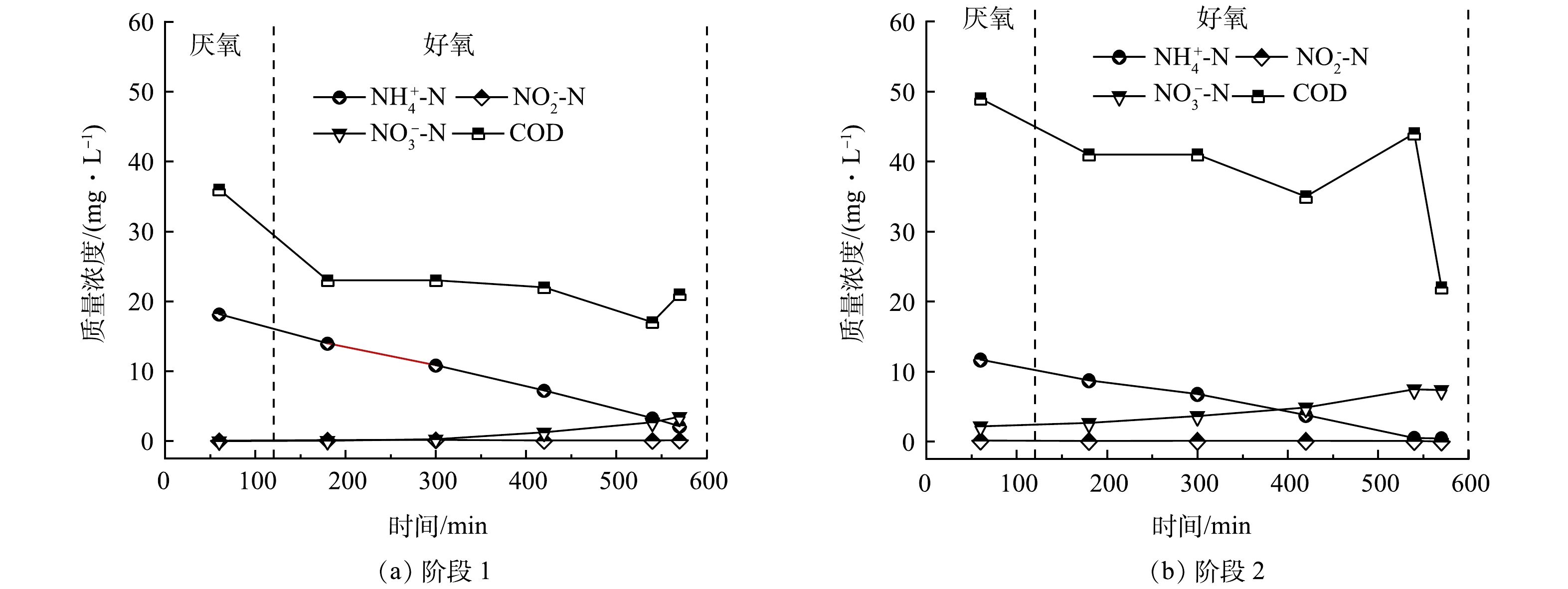
对两阶段进行了单周期采样(分别在第23天和第49天),水质浓度变化如图3所示。由图3可知,阶段1COD的去除主要发生在厌氧阶段,且COD值较低。而氨氮浓度随着反应时间呈现线性降低的趋势,其去除速率为0.031 mg·(L·min)−1。而在此阶段亚硝酸盐浓度几乎未检出,硝酸盐浓度在实验后期420 min略有升高,表明厌氧氨氧化脱氮效果良好。而在阶段2时在反应器中COD值较高,这可能是由于进水为实际废水,其可生物降解性有机物浓度低。与阶段1相同,COD的去除主要发生在厌氧阶段,氨氮在反应器内浓度较阶段1偏低,去除速率为0.022 mg·(L·min)−1。受进水有机物浓度较低等因素影响,与阶段1相比硝酸盐浓度较高。
-
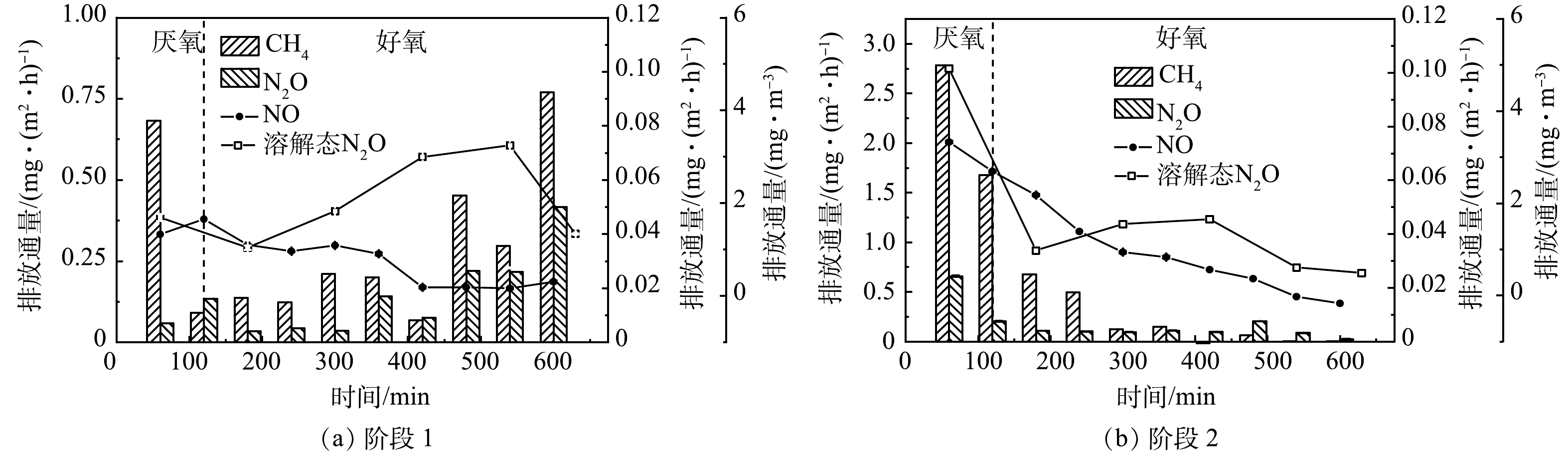
MABR单周期气体排放如图4所示,阶段1,气态CH4和N2O的排放量较为平缓,在厌氧阶段和好氧阶段末气态CH4排放较高,排放通量分别为0.6 mg·(m2·h)−1和0.77 mg·(m2·h)−1。气态N2O的排放在实验过程中变化幅度较小,气态N2O排放可能受溶解态N2O影响,在420-540 min时溶解态N2O浓度升高至2.99~3.24 mg·m−3,随后在600 min气态N2O升高至0.42 mg·(m2·h)−1,气态N2O的释放较溶解态N2O峰值约滞后60~180 min,这主要由于溶解性N2O的逐步产生与释放过程。气态NO与气态N2O存在较好的正相关性,相关系数数R为0.96,这可能是由于厌氧阶段反硝化为N2O的主要排放源,当进水碳源不足时,NO、N2O还原反应不完全,存在一定气态NO、N2O积累,导致监测气体中NO、N2O浓度高。
阶段2,厌氧阶段是主要的CH4和N2O排放源,厌氧阶段气态CH4和N2O排放通量分别为2.78和0.66 mg·(m2·h)−1,并在随后的好氧初期仍存在较高的气态CH4排放,厌氧阶段末期溶解性N2O浓度达到4.92 mg·m−3。厌氧阶段气态NO、溶解态N2O与气态N2O变化规律相似,随着COD的消耗,均表现出降低趋势。气态NO与气态N2O相关系数R为0.96。好氧阶段气态N2O和CH4排放平缓,最高排放通量分别为0.66和2.78 mg·(m2·h)−1,而NO排放通量随着时间逐步降低。溶解态N2O排放通量在420 min存在升高现象,但气态N2O排放通量在480 min左右升高,与阶段1相似,气态N2O较溶解态N2O峰值滞后约60 min。
KINH等的研究表明MABR采用无泡曝气技术,N2O主要以溶解态形式赋存,其气态释放量较低[20]。本研究中溶解态N2O浓度为0.49~4.90 mg·m−3略低于KINH等[20]的报道值((11±1) mg·m−3)。同时KINH[21]指出MABR中好氧生物膜是N2O和NO的产生热区,受进水碳源等影响,生物膜由内向外N2O和NO浓度逐步降低,导致其N2O排放量低。生物膜内N2O的分布及其影响因素需要开展进一步研究。
根据生物脱氮过程N2O的排放路径,厌氧阶段主要由反硝化反应产生,而好氧阶段主要由硝化反应产生[22]。DUAN等[23]指出硝化反应产生的N2O与硝化速率成正相关关系,阶段1和二氨氮氧化速率分别为0.03 mg·(L·min)−1和0.02 mg·(L·min)−1,因此,阶段1好氧阶段气态和溶解态N2O浓度均高于阶段2。阶段2厌氧阶段CH4和N2O排放量较高,可能与COD值以及反硝化作用有关。LIU等[24]利用模型探究了在不同条件下MABR的N2O的释放情况,结果表明,在较低COD值(≤280 mg·L−1)以下时,随着COD值的上升N2O排放量升高。
所监测温室气体的排放因子如图5所示。在厌氧阶段时CH4、N2O和NO的排放因子分别为(0.010 3±0.010 5)%、(0.005 0±0.005 5)%、(0.001 0±0.000 4)%。而在好氧阶段时CH4、N2O和NO的排放因子分别为(0.001 5±0.001 7)%、(0.002 1±0.001 5)%以及(0.000 5±0.000 2)%。本实验测得的N2O排放因子与KINH在MABR中测得的(0.005 8±0.000 5)%[20]结果类似,低于NI等[25]采用一维模型对MABR排放NO和N2O的模拟值(3.5%)。本研究中,MABR中温室气体的释放主要发生在厌氧阶段,反硝化反应可能是驱动N2O产生与释放的主要来源,由NO至N2O还原反应不完全而产生的N2O释放,同时该阶段CH4排放量高,需要进一步探究厌氧阶段N2O和CH4同步减排的有效方法。好氧阶段通过亚硝化-厌氧氨氧化反应脱氮[12],可能由于亚硝化-厌氧氨氧化反应在膜曝气生物膜上发生,溶解性的气态产物可被快速的转化,因此,好氧阶段不是气体排放的主要阶段,这与活性污泥系统气体排放[6]差异较大。
水质指标与气体排放情况的相关性分析如图6所示。由图6可知,在2个阶段中,CH4、N2O和NO的排放浓度与水体中氨氮浓度呈正相关,与氨氮去除率呈现负相关。说明当水体中氨氮积累越多,气体的排放量越大。而水体中硝酸盐浓度与CH4、N2O和NO的排放浓度呈负相关关系。硝酸盐主要来自于硝化反应和厌氧氨氧化反应,表明硝化反应可能不是本工艺N2O产生的主要来源。该现象与DUAN等[23]的研究结果一致。气态NO和N2O存在正相关关系,气态NO是反硝化过程N2O的前体物,对反硝化过程N2O的释放具有指示作用。
-
1)通过构建的MABR工艺实现了有机物和氮的高效去除,生活污水中的芳香蛋白类物质得到明显去除,通过自养脱氮实现了氨氮和TN的高效去除。阶段1 C/N比为3.00±0.14时,COD、NH4+-N和TN去除率分别为85.24%、90.10%和64.35%,阶段2 C/N比为1.67±0.07时,COD、NH4+-N和TN去除率分别为75.39%、96.39%和81.88%。
2)MABR中,溶解态N2O的峰值先于气态N2O出现,两阶段溶解态N2O浓度最高可达3.247 7 和4.923 2 mg·m−3。CH4和N2O的排放主要发生在厌氧阶段,厌氧阶段CH4、N2O和NO的排放因子分别为(0.010 3±0.010 5)%、(0.005 0±0.005 5)%、(0.001 0±0.000 4)%。而在好氧阶段CH4、N2O和NO的排放因子分别为(0.001 5±0.001 7)%、(0.002 1±0.001 5)%以及(0.000 5±0.000 2)%,反硝化反应可能是本工艺中N2O排放的主要生物反应来源。
膜曝气生物膜反应器处理生活污水N2O等温室气体的排放特性
Emission characteristics of N2O and other greenhouse gases from membrane aerated biofilm reactor treating domestic wastewater
-
摘要: 针对生活污水处理减污降碳的需求,本研究采用膜曝气生物膜反应器(membrane aerated biofilm reactor, MABR)耦合厌氧氨氧化工艺处理低碳氮比生活污水,考察了水质污染物去除的同时,分析了甲烷(CH4)、氧化亚氮(N2O)和一氧化氮(NO)的排放特性。结果表明,MABR实现了较好的碳氮污染物去除效果,当处理进水C/N为3.00±0.14的模拟污水时,COD、NH4+-N和TN去除率分别为85.24%、90.10%和64.35%;当处理进水C/N为1.67±0.07的实际污水时,COD、NH4+-N和TN去除率分别为75.39%、96.39%和81.88%。MABR具有较低的CH4和N2O排放因子,厌氧阶段分别为(0.010 3±0.010 5)%、(0.005 0±0.005 5)%,好氧阶段分别为(0.001 5±0.001 7)%、(0.002 1±0.001 5)%,厌氧阶段是CH4和N2O排放的主要阶段。气态NO和气态N2O存在正相关关系,反硝化反应可能是N2O产生的主要路径。NO是反硝化过程N2O产生的前体物,对反硝化过程N2O的释放具有指示作用。Abstract: In this study, a membrane aerated biofilm reactor (MABR) coupled with anaerobic ammonia oxidation process was used to treat domestic wastewater with low carbon to nitrogen ratio in order to meet the demand for reduction of pollutant and carbon emission. This study investigated the removal of pollutants in wastewater and the emission characteristics of methane (CH4), nitrous oxide (N2O) and nitric oxide (NO). The results showed that the MABR achieved a good performance on carbon and nitrogen pollutant removal. When treating synthetic wastewater with C/N of 3.00±0.14, the COD, NH4+-N and TN removal efficiencies were 85.24%, 90.10% and 64.35%, respectively; when treating real domestic wastewater with C/N of 1.67±0.07, the COD, NH4+-N and TN removal efficiencies were 75.39%, 96.39% and 81.88%, respectively. The MABR had low CH4 and N2O emission factors of (0.010 3±0.010 5)% and (0.0050±0.0055)% in anaerobic stage and (0.001 5±0.001 7)% and (0.002 1±0.001 5)% in the aerobic stage, respectively, indicating anaerobic stage was the main source for CH4 and N2O emissions. Gaseous NO was positively corelated with gaseous N2O. Denitrification could be the main pathway of N2O production. Gaseous NO was the precursor of N2O production during denitrification process, which could indicate N2O emission accordingly.
-
-
表 1 MABR不同阶段进水水质和处理效果
Table 1. The influent concentration and treatment efficiency of MABR at different stages
阶段 进水(mg·L−1) 出水(mg·L−1) 去除率/% COD NH4+-N TN COD NH4+-N TN COD NH4+-N TN 阶段1 115±1.41 39.1±0.92 39.1±0.92 17±4.24 3.89±2.22 15.72±4.96 85.24±3.51 90.1±5.61 64.35±16.49 阶段2 64±12.73 38.44±4.27 49.39±3.34 16±5.66 1.39±1.15 8.86±2.71 75.39±3.95 96.39±2.89 81.88±7.55 -
[1] 郝晓地, 杨振理, 于文波, 等. 污水处理过程N2O排放: 过程机制与控制策略[J]. 环境科学, 2023, 44(2): 1163-1173. [2] 梁小玲, 李平, 吴锦华, 等. 短程同步硝化反硝化过程的脱氮与N2O释放特性[J]. 环境科学, 2013, 34(5): 1845-1850. [3] DUAN H R, ZHAO Y F, KOCH K, et al. Insights into nitrous oxide mitigation strategies in wastewater treatment and challenges for wider implementation[J]. Environmental Science & Technology, 2021, 55(11): 7208-7224. [4] 闫旭, 邱德志, 郭东丽, 等. 中国城镇污水处理厂温室气体排放时空分布特征[J]. 环境科学, 2018, 39(3): 1256-1263. doi: 10.13227/j.hjkx.201706079 [5] KAMPSCHREUR M J, TEMMINK H, KLEEREBEZEM R, et al. Nitrous oxide emission during wastewater treatment[J]. Water Research, 2009, 43(17): 4093-4103. doi: 10.1016/j.watres.2009.03.001 [6] 韩海成, 周东, 王亚宜, 等. 城市污水A2/O处理系统好氧池N2O和NO的释放特征及影响因素[J]. 中国环境科学, 2016, 36(2): 398-405. [7] GU J, YANG Q, LIU Y. Mainstream anammox in a novel A-2B process for energy-efficient municipal wastewater treatment with minimized sludge production[J]. Water Research, 2018, 138(1): 1-6. [8] JETTEN M S M, WAGNER M, Fuerst J, et al. Microbiology and application of the anaerobic ammonium oxidation (‘anammox’) process[J]. Current Opinion in Biotechnology, 2001, 12(3): 283-288. doi: 10.1016/S0958-1669(00)00211-1 [9] JI J, PENG Y, LI X, et al. A novel partial nitrification-synchronous anammox and endogenous partial denitrification (PN-SAEPD) process for advanced nitrogen removal from municipal wastewater at ambient temperatures[J]. Water Research, 2020, 175: 115690. doi: 10.1016/j.watres.2020.115690 [10] 陈瑜. 基于MABRs亚硝化过程的高氨氮废水处理研究[D]. 哈尔滨: 哈尔滨工业大学, 2018. [11] AUGUSTO M R, CAMILOTI P R, SOUZA T S O. Fast start-up of the single-stage nitrogen removal using anammox and partial nitritation (SNAP) from conventional activated sludge in a membrane-aerated biofilm reactor[J]. Bioresource Technology, 2018, 266: 151-157. doi: 10.1016/j.biortech.2018.06.068 [12] 宋舒兴, 隋倩雯, 高超龙, 等. 膜曝气生物膜反应器耦合厌氧氨氧化工艺处理低C/N比生活污水[J]. 环境科学学报, 2023, 43(4): 208-216. doi: 10.13671/j.hjkxxb.2022.0396 [13] CHANG M, LIANG B, ZHANG K, et al. Simultaneous shortcut nitrification and denitrification in a hybrid membrane aerated biofilms reactor (H-MBfR) for nitrogen removal from low COD/N wastewater[J]. Water Research, 2022, 211: 118027. doi: 10.1016/j.watres.2021.118027 [14] CZEPIELl P, CRILL P, HARRISS R. NITROUS. Oxide emissions from municipal wastewater treatment[J]. Environmental Science & Technology, 1995, 29(9): 2352-2356. [15] 张羽, 秦晓波, 廖育林, 等. 亚热带农业小流域水系N2O扩散通量及其影响因素[J]. 农业工程学报, 2016, 32(7): 215-223. [16] CZEPIELl P F, CRILL P F R, HARRISS R. Nitrous oxide emissions from municipal wastewater treatment[J]. Environmental Science and Technology, 1995, 29(9): 2352-2356. doi: 10.1021/es00009a030 [17] CHEN W, WESTERHOFF P, LEENHEER J A, et al. Fluorescence excitation−emission matrix regional Integration to quantify spectra for dissolved organic matter[J]. Environmental Science & Technology, 2003, 37(24): 5701-5710. [18] 杨金强, 赵南京, 殷高方, 等. 城市生活污水处理过程三维荧光光谱在线监测分析方法[J]. 光谱学与光谱分析, 2020, 40(7): 1993-1997. [19] STROUS M, PELLETIER E, MANGENOT S, et al. Deciphering the evolution and metabolism of an anammox bacterium from a community genome[J]. Nature, 2006, 440(7085): 790-794. doi: 10.1038/nature04647 [20] KINH C T, SUENAGA T, HORI T, et al. Counter-diffusion biofilms have lower N2O emissions than co-diffusion biofilms during simultaneous nitrification and denitrification: Insights from depth-profile analysis[J]. Water Research, 2017, 124: 363-371. doi: 10.1016/j.watres.2017.07.058 [21] KINH C T, RIYA S, HOSOMI M, et al. Identification of hotspots for NO and N2O production and consumption in counter- and co-diffusion biofilms for simultaneous nitrification and denitrification[J]. Bioresource Technology, 2017, 245: 318-324. doi: 10.1016/j.biortech.2017.08.051 [22] DUAN H, ZHAO Y, KOCH K, et al. Insights into nitrous oxide mitigation strategies in wastewater treatment and challenges for wider implementation[J]. Environmental Science and Technology, 2021, 55(11): 7208-7224. doi: 10.1021/acs.est.1c00840 [23] DUAN H, VAN D A B, THWAITES B J, et al. Mitigating nitrous oxide emissions at a full-scale wastewater treatment plant[J]. Water Research, 2020, 185: 116196. doi: 10.1016/j.watres.2020.116196 [24] LIU Y, ZHU T, REN S, et al. Contribution of nitrification and denitrification to nitrous oxide turnovers in membrane-aerated biofilm reactors (MABR): A model-based evaluation[J]. Science of the Total Environment, 2022, 806: 151321. doi: 10.1016/j.scitotenv.2021.151321 [25] NI B, SMETS B F, YUAN Z, et al. Model-based evaluation of the role of Anammox on nitric oxide and \nitrous oxide productions in membrane aerated biofilm reactor[J]. Journal of Membrane Science, 2013, 446: 332-340. doi: 10.1016/j.memsci.2013.06.047 -
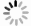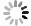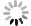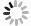


 下载:
下载: